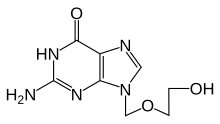
ABACAVIR
Abacavir


Nombre (IUPAC) sistemático
(1S,4R)-4-[2-amino-6-(ciclopropilamino)- 9H-purina-9-il]-2-ciclopenteno-1-metanol sulfato (sal)
Identificadores
Número CAS 136470-78-5
Código ATC J05AF06 J05AF06
Datos químicos
Fórmula C14H18N6O
Peso mol. 286.333 g/mol
Farmacocinética
Metabolismo Hígado
Excreción Renal (1.2% abacavir, 30% 5'-metabolito del ácido carboxílico, 36% 5'-metabolito glucurónido, 15% otros metabolitos menores). Heces (16%)
Datos clínicos
Cat. embarazo ?
Estado legal ?
Vías de adm. Oral
El sulfato de abacavir, también conocido como 1592U89, es un fármaco carboxílico sintético análogo de los nucleósidos, inhibidor de la transcriptasa inversa, que es utilizado en el tratamiento contra el VIH, causante del sida. Existe una marca comercial que se expende en combinación con otros fármacos antivirales (abacavir, zidovudina y lamivudina). Fue aprobado para uso público en 1998.
Indicaciones
El fármaco es usado para tratar el HIV tipo 1 y debe siempre ser utilizado en combinación con otros agentes antirretrovirales. Abacavir jamás debe usarse como único prospecto cuando se cambien los regímenes antirretrovirales debido a pérdida de la respuesta viral.
[editar]Mecanismo de acción
El abacavir es un análogo de la guanosina (una purina). Su objetivo es la inhibición de la enzima transcriptasa inversa.
Farmacocinética
El abacavir se administra por vía oral y posee una elevada biodisponibilidad, de alrededor del 83%. Es metabolizado por medio de una de dos enzimas, la alcohol deshidrogenasa o por la gluconil transferasa. Se ha observado que el fármaco atraviesa la barrera hematoencefálica. Se considera que alcanza concentraciones en líquido cefalorraquídeo similares a las de zidovudina, por lo que presenta una buena penetración en elsistema nervioso central y por lo que actualmente se hacen pruebas preliminares para ser utilizado en el tratamiento del complejo de demenciaasociado al virus de la inmunodeficiencia humana.
Interacciones
Analgésicos: el abacavir posiblemente reduce la concentración plasmática de metadona.
Antibacterianos: la concentración plasmática de abacavir se reduce posiblemente por la rifampicina.
Antiepilépticos: la concentración plasmática de abacavir se reduce posiblemente por la fenitoína.
Antivíricos: la concentración plasmática de abacavir se reduce por el tripanavir.
Barbitúricos: la concentración plasmática de abacavir se reduce posiblemente por el fenobarbital.1
Reacciones adversas
Se ha asociado al fármaco la aparición de una reacción fatal de hipersensibilidad. Los síntomas incluyen fiebre, rash cutáneo, fatiga, síntomas gastrointestinales como náusea, vómito, diarrea o dolor abdominal. Otros síntomas son de tipo respiratorio como faringitis, disnea o tos. La hipersensibilidad está relacionada con el HLA-B*57012 3 para el cual existe en muchos países occidentales una prueba disponible que permite reducir la incidencia de reacciones de hipersensibilidad debido al HLA-B*5701.4
Precauciones especiales
 Tabletas de Abacavir.
Tabletas de Abacavir.Los médicos tratantes deben aconsejar a los pacientes que descontinúen el fármaco si aparece un signo posible de alergia o sensibilidad al abacavir, ya que se han presentado casos de fallecimientos debido a esta eventualidad. Otros fallecimientos se han asociado a daño agregado al hígado en personas con problemas hepáticos, ya que esta droga agrava una condición preexistente. Raras veces se ha presentado acidosis láctica con el uso de análogos de nucleósidos.
El uso de fármacos antivirales puede provocar en los pacientes bajo tratamiento una acumulación de la grasa corporal, sobre todo en piernas, brazos y en la base del cuello. Abacavir nunca debe ser administrado a niños menores de tres meses.
Teratogenicidad
Los estudios de carcinogenicidad realizados con abacavir administrado oralmente en ratones y ratas, mostraron un aumento en la incidencia de tumorestanto malignos como no malignos. Los tumores malignos ocurrieron en la glándula prepucial de los animales machos y en la glándula clitoral de las hembras de ambas especies, y en el hígado, vejiga urinaria, ganglios linfáticos y subcutis de las ratas hembras.5
Sobredosificación
Son pocos los datos acerca de sobredosificación por abacavir. Las víctimas por sobredosis deben ser llevadas al centro toxicológico local o al departamento de urgencias hospitalarias para instalar un tratamiento. Se aconseja llevar consigo la botella o empaque del medicamento.
Presentaciones y formas farmacéuticas
El sulfato de abacavir se presenta en forma de tabletas y solución oral.6
Tabletas conteniendo 300 mg de abacavir. Tambien existen asociaciones con otros antiretroviraes como Lamivudina, conteniendo 300 mg de éste último y 600 mg de Abacavir (comercialzado por Humax Pharmaceutical en Colombia como Lamcavir).
Solución oral conteniendo 20 mg por mililitro y con sabor artificial agregado.